在科學、技術和醫學的交叉領域,尋找可行的藥物是最艱巨的挑戰之一。從數學上講,隨機偶然發現一個好的治療候選者的可能性小得驚人。這主要是因為只有幾個原子可以通過大量的方法連接在一起,使初看起來像藥物一樣的化合物。
在對這些分子進行更深入的檢查后,絕大多數分子都會成為不適合的治療方法。臨床上可行的藥物必須具有多種特性或特性,如果缺少其中任何一種特性或特性或超出范圍,則可能會使藥物無效,甚至有毒。藥物獵人尋求的特性示例包括描述藥物的結合親和力、溶劑性、膜滲透性、分子量和穩定性的特性,等等。
從本質上講,候選藥物的追求是多目標優化問題。
生成式 AI 模型,例如 NVIDIA BioNeMo 中的 MolMIM,旨在直接解決尋找具有正確屬性的分子的挑戰。使用 MolMIM,研究人員可以生成分子,以最大限度地提高用戶指定的評分函數(簡稱 Oracle 函數)。MolMIM 執行受控生成,在用戶提供的 Oracle 函數的指導下,瀏覽化學空間的學習內部表示。
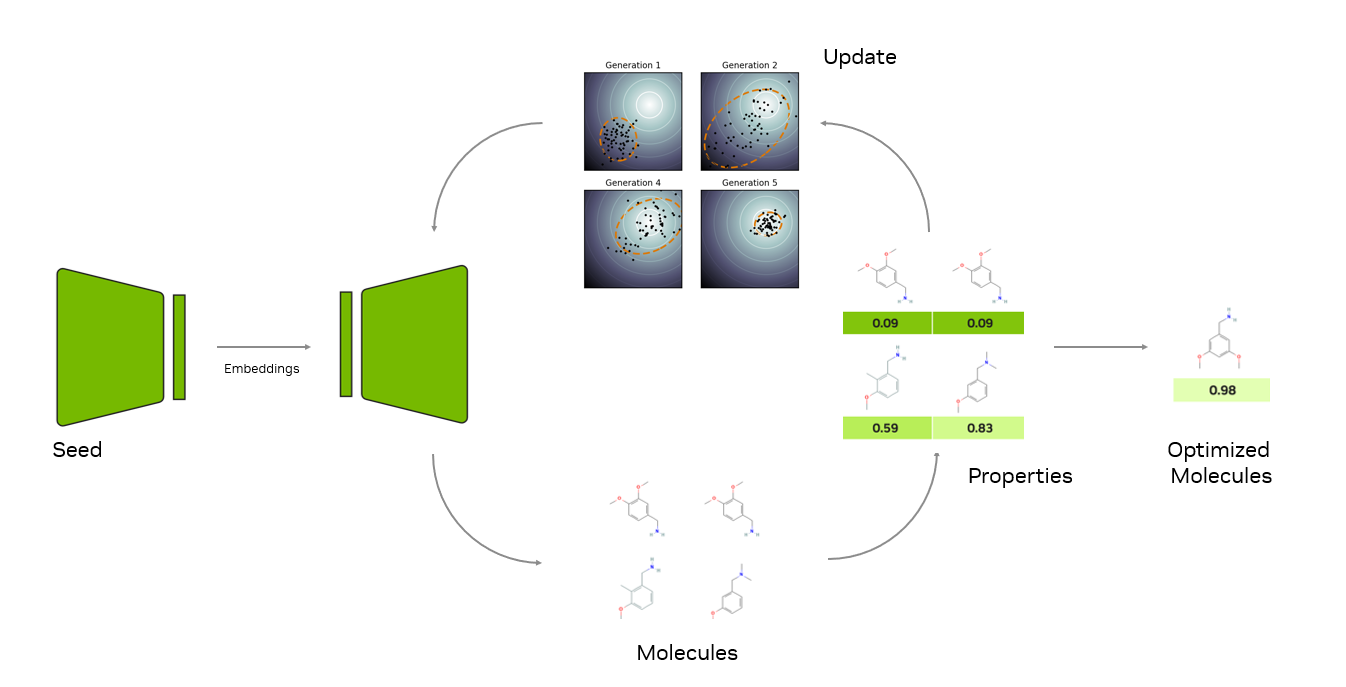
研究人員可以定義他們想要的任何目標函數,甚至是計算多個目標的函數。在幕后,MolMIM 使用名為 CMA-ES 的無梯度數值優化算法來瀏覽模型的潛在空間。生成過程是迭代的:
- 在每次迭代中,MolMIM 都會生成一批分子。
- 借助用戶提供的 Oracle 函數,計算分子的屬性。
- 然后,使用協方差矩陣適應進化策略 (CMA-ES) 更新隱向量,以生成下一批分子。
- 算法會一直持續到收。
使用 BioNeMo Cloud API 和 BioNeMo 的 Python 客戶端庫,優化分子生成工作流程非常簡單。要定義 Oracle 函數,您只需編寫一個遵循簡單調用簽名的 Python 函數即可。該函數應獲取 SMILES 列表,并返回相同長度的分數 NumPy 數組。通過定義 Oracle 函數,可以從 BioNeMo Python 客戶端實例化優化器,并開始分子生成!
您可以通過 BioNeMo 的 Cloud API 搶先體驗 MolMIM,該 API 將于 2024 年 1 月 19 日發布。
此外,BioNeMo 的 Cloud API 將加速更新 DiffDock,這是一種 AI 模型,用于預測蛋白質 – 配體復合體的三維結構,這在藥物研發過程中是一個關鍵步驟。通過 BioNeMo 的 DiffDock 更新版,研究人員能夠以超過相同硬件上基準實現的 2.5 倍速度預測蛋白質 – 配體復合體的三維姿態。有關更多信息,請參閱借助 NVIDIA BioNeMo 服務為藥物研發構建生成式 AI 流程。
注冊搶先體驗 NVIDIA BioNeMo Cloud API,或立即開始使用BioNeMo 框架進行模型訓練。
?